Симметрия в химии проявляется в геометрической конфигурации молекул, что сказывается на специфике физических и химических свойств молекул в изолированном состоянии, во внешнем поле и при взаимодействии с другими атомами и молекулами.
Большинство простых молекул обладает элементами пространственной симметрии равновесной конфигурации: осями симметрии, плоскостями симметрии.
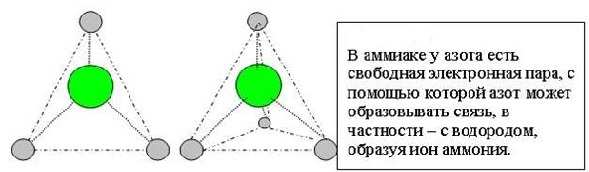
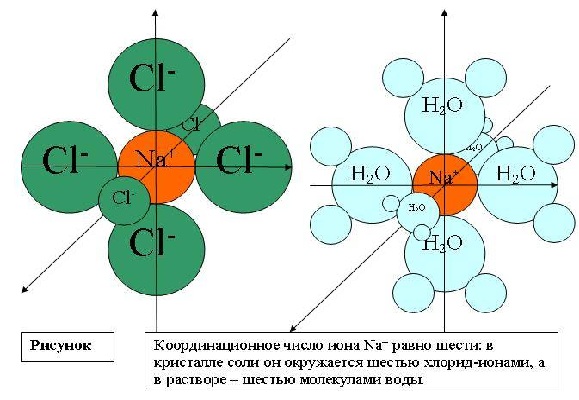
Исключительно важную роль в мире живой природы играют молекулы ДНК (дезоксирибонуклеиновая кислота). Это двуцепочечный высокомолекулярный полимер, мономером которого являются нуклеотиды. Молекулы ДНК имеют структуру двойной спирали, построенной по принципу комплементарности. 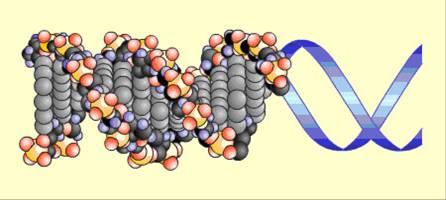
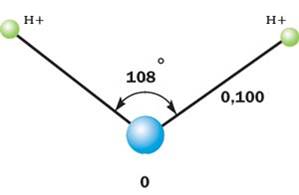
Молекула воды имеет симметричную V-образную форму, так как два небольших атома водорода располагаются с одной стороны от сравнительно крупного атома кислорода. Это сильно отличает молекулу воды от линейных молекул, например Н2Ве, в которой все атомы располагаются цепочкой. Именно такое странное расположение атомов в молекуле воды и позволяет ей иметь множество необычных свойств.
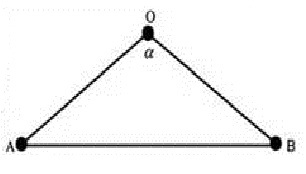
Если внимательно рассмотреть геометрические параметры молекулы воды, то в ней обнаруживается определенная гармония. Чтобы увидеть ее, построим равнобедренный треугольник Н-О-Н с протонами в основании и кислородом в вершине. Такой треугольник схематично копирует структуру молекулы воды.
В ней есть симметрия, которая играет основную роль в попытках всестороннего объяснения физического мира, и асимметрия, наделяющая эту молекулу возможностью движения и связью с золотой пропорцией.
"Золотой треугольник". Соотношение его сторон OA:AB = OB:AB =0,618, угол при верши не ? = 108°.
Исследователи золотой пропорции с античных времен до наших дней всегда восхищались и продолжают восхищаться ее свойствами, которые проявляются в строении различных элементов физического и биологического мира. Золотая пропорция обнаруживается везде, где соблюдены принципы гармонии.
|
При химических реакциях, подтвержденных впоследствии обширным экспериментальным материалом и оказавших большое влияние на развитие препаративной органической химии принцип утверждает, что отдельные элементарные акты химических реакций проходят с сохранением симметрии молекулярных орбиталей, или орбитальной симметрии. Чем больше нарушается симметрия орбиталей при элементарном акте, тем труднее проходит реакция.
Учёт симметрии молекул важен при поиске и отборе веществ, используемых при создании химических лазеров и молекулярных выпрямителей, при построении моделей органических сверхпроводников, при анализе канцерогенных и фармакологически активных веществ и т. д.
|